Tecnovigilancia: seguridad para la salud
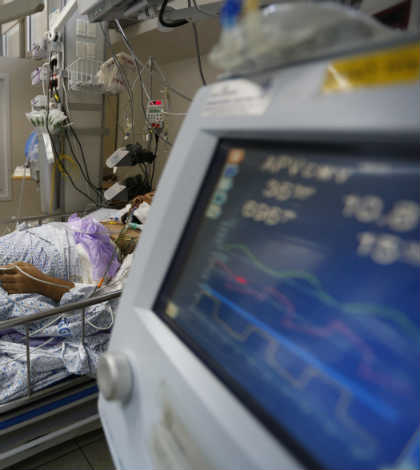
La tecnovigilancia tiene como propósito garantizar que los dispositivos médicos que se encuentran disponibles en el mercado funcionen de la manera indicada, conforme a la intención de uso del fabricante y, en caso contrario, se corrija para disminuir la probabilidad de incidentes.
Por: René Menchaca, Emma Escandón y Raúl de la Cerda*
La creciente complejidad de los sistemas sanitarios, tanto en los procedimientos como en los dispositivos médicos, puede provocar errores que afecten la salud, por lo que deben establecerse las medidas necesarias como la tecnovigilancia, para evitarlos y/o minimizarlos.
La tecnovigilancia tiene como propósito garantizar que los dispositivos médicos (sustancia, material, aparato o instrumento empleado en el diagnóstico, tratamiento, monitoreo o prevención de enfermedades en humanos) que se encuentran disponibles en el mercado funcionen de la manera indicada, conforme a la intención de uso del fabricante y, en caso contrario, se tomen las acciones correspondientes para corregir y/o disminuir la probabilidad de incidentes.
Para hacer efectiva la tecnovigilancia se estableció en octubre de 2012 la NOM-240-SSA1-2012, Instalación y Operación de la Tecnovigilancia, la cual entró en vigor a finales de abril pasado. Esta norma plantea los lineamientos sobre los cuales se deben realizar las actividades de la tecnovigilancia, con la finalidad de garantizar la protección de la salud del paciente y la seguridad de los productos.
La norma no tiene como objetivo sancionar a los profesionales de la salud involucrados en el incidente adverso, sino evitar la repetición. El titular del Registro Sanitario tiene la obligación de presentar el informe de tecnovigilancia como parte del procedimiento de la renovación de cada Registro Sanitario de Dispositivos Médicos, en caso contrario no se dará renovación y perderá la autorización sanitaria para comercializar el producto en México.
La tecnovigilancia es un procedimiento establecido a nivel internacional por las autoridades sanitarias correspondientes (FDA, Comunidad Económica Europea, Health Canadá). En México, la NOM 240 establece que se deben generar diversos procedimientos normativos de operación que garanticen que el representante legal cuenta con procesos para recibir, registrar, investigar, identificar y clasificar las notificaciones de incidentes adversos y comunicar las acciones tomadas para que no se vuelvan a presentar.
Tomando en cuenta que los incidentes adversos, generalmente, se presentan en las instituciones de salud y que la mayor parte de los dispositivos médicos se encuentran operando en hospitales, es indispensable la participación de los profesionales para la detección de fallas; los procedimientos que deben seguirse están estipulados en la NOM 240, en donde además se indica que se requiere de un responsable de tecnovigilancia para que sea el único interlocutor ante la autoridad sanitaria.
No obstante, debido al desarrollo de la tecnología, es frecuente encontrar dispositivos médicos operando en los hogares como es el caso de los glucómetros, medidores de presión sanguínea y equipos de diálisis peritoneal, por mencionar algunos, por lo que existe el riesgo de que se presenten incidentes adversos durante su operación; si es al caso, los pacientes y familiares pueden notificar los incidentes a la autoridad sanitaria nacional: Comisión Federal para la Protección Contra Riesgos Sanitarios (Cofepris) y/o Centro Nacional de Farmacovigilancia (CNFV).
La seguridad de la operación de los dispositivos médicos involucra al fabricante, personal de salud, pacientes y familiares, por lo que es importante un adecuado conocimiento y aplicación de la tecnovigilancia.
*René Menchaca es socio del Sector Salud de PwC México ([email protected])
Emma Escandón y Raúl de la Cerda son especialistas de la práctica de Dispositivos Médicos de PwC México
Contacto:
www.pwc.com/mx
Facebook: PwCMexico
Twitter: @PwC_Mexico
Blog: pwc.mx
Youtube: PwCMx
*Las opiniones expresadas son sólo responsabilidad de sus autores y son completamente independientes de la postura y la línea editorial de Forbes México.
















